Sieben herausragende Datenressourcen, Software-Tools und begutachtete Publikationen unserer Mitglieder wurden als SIB Remarkable Outputs – eine jährliche Würdigung der Exzellenz und Vielfalt der Leistungen im Bereich der Bioinformatik in der Schweiz.
Möchten Sie nächstes Jahr zu den ausgewählten Outputs gehören? Die nächste Einreichungsfrist finden Sie auf der Seite Remarkable Outputs.
-
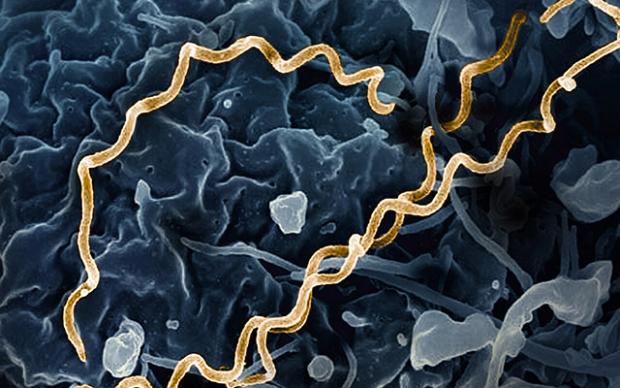
Ein schnelles Suchwerkzeug für biologische Sequenzen
Veröffentlicht in: Nature
Beteiligte SIB-Gruppe: Biomedizinische Informatik unter der Leitung von Gunnar Rätsch an der ETH Zürich
Beschreibung: MetaGraph findet innerhalb von Sekunden spezifische DNA-, RNA- und Proteinsequenzen in Millionen öffentlicher Datensätze. Wie eine gewöhnliche Internet-Suchmaschine indexiert und durchsucht das skalierbare Tool effizient riesige globale Datensätze – und setzt damit einen neuen Standard für die groß angelegte Erforschung von Sequenzierungsdaten.
Das Komitee sagte: „MetaGraph löst einen großen Engpass: die Fähigkeit, schnell wachsende Mengen an Sequenzierungsdaten zu durchsuchen und zu erkunden. Sein herausragender technischer Beitrag verändert die Art und Weise, wie Wissenschaftler groß angelegte biologische Daten untersuchen, und beschleunigt Entdeckungen in vielen Bereichen der Lebenswissenschaften.“
Entdecken Sie diese Veröffentlichung
-
Ein Tool zur Bewertung von durch KI vorhergesagten makromolekularen Komplexen
Veröffentlicht in: Nature Methods
Beteiligte SIB-Gruppe: Computational Structural Biology unter der Leitung von Torsten Schwede an der Universität Basel
Beschreibung: Neue KI-Tools können die Struktur grosser biologischer Komplexe aus Proteinen, DNA und kleinen Molekülen vorhersagen. OpenStructure bewertet die Genauigkeit solcher Vorhersagen anhand experimentell ermittelter Strukturen durch einen reproduzierbaren, transparenten und skalierbaren Arbeitsablauf.
Das Komitee sagte: „OpenStructure stellt einen bedeutenden Fortschritt für die Strukturbiologie und Benchmarking-Verfahren dar, indem es ein robustes, vollautomatisiertes System zur Bewertung von KI-gestützten Strukturvorhersagemethoden der nächsten Generation etabliert. Das System ist bereits in die Benchmarking-Bemühungen der Fachgemeinschaft integriert, was seine Relevanz und Wirkung unterstreicht.“
-
Eine Methode zur Erkennung von Elternteil-spezifischen Effekten auf Merkmale
Veröffentlicht in: Nature
Beteiligte SIB-Gruppe: Gruppe fürstatistische Genetik unter der Leitung vonProf. Zoltán Kutalik an der Universität Lausanne
Beschreibung: Es zeigte sich, dass Stoffwechsel , Krankheitsrisiko und andere Merkmale sich in unterschiedliche – und sogar entgegengesetzte – Richtungen verschieben, je nachdem, ob eine genetische Variante von der Mutter oder vom Vater stammt. Die Studie nutzte einen neuartigen Ansatz, um Eltern-Herkunfts-Effekte in großen menschlichen Gen-Datensätzen zu analysieren.
Stellungnahme des Komitees: „Dieser analytische Rahmen ermöglicht die systematische Untersuchung eines wichtigen, aber oft übersehenen evolutionären Phänomens. Die Fähigkeit, die elterliche Herkunft von Allelen anhand begrenzter Stammbaumdaten abzuleiten, stellt einen bedeutenden Beitrag zur statistischen Genetik und Bioinformatik dar.“
Entdecken Sie diese Veröffentlichung
-
Eine Ressource zum Darmmikrobiom auf Unterartenebene
Veröffentlicht in: Cell Host & Microbe
Beteiligte SIB-Gruppe: Computational Evolutionary Genomics unter der Leitung von Evgeny Zdobnov und Evgenia Kriventseva an der Universität Genf
Beschreibung: Der erste umfassende Genomkatalog menschlicher Darmmikroben auf Unterartenebene erfasst genetische Variationen innerhalb einer Art, die bei Standardanalysen übersehen werden. Machine-Learning-Modelle, die HuMSub-Unterartenprofile nutzten, sagten Darmkrebs anhand von Stuhlproben genauer voraus als Modelle auf Artenebene.
Das Komitee sagte: „HuMSub behebt eine seit langem bestehende Einschränkung der Mikrobiomforschung. Durch die Unterscheidung von Unterarten innerhalb derselben Art und die Verknüpfung dieser Unterschiede mit funktionellen und krankheitsbezogenen Merkmalen ermöglicht der Ansatz eine präzisere biologische Interpretation von Mikrobiomdaten.“
Entdecken Sie diese Veröffentlichung
-
Ein Werkzeug zur Erforschung der Evolution anhand von 3D-Proteinstrukturen
Veröffentlicht in: Nature Structural & Molecular Biology
Beteiligte SIB-Gruppe: Comparative Genomics unter der Leitung von Christophe Dessimoz ( ) an der Universität Lausanne
Beschreibung: FoldTree deckt Beziehungen zwischen Proteinen auf, indem es deren dreidimensionale Strukturen statt ihrer genetischen Sequenzen vergleicht. Dieser neuartige Ansatz ermöglicht es Wissenschaftlern, alte Evolutionsgeschichten nachzuverfolgen, die mit traditionellen sequenzbasierten Methoden nur schwer zu erkennen sind.
Das Komitee sagte: „FoldTree zeigt, wie ein bahnbrechender Durchbruch in einem Bereich – in diesem Fall die KI-basierte Vorhersage von Proteinstrukturen – dazu beitragen kann, eine seit langem bestehende Herausforderung in einem anderen Bereich anzugehen. Seine innovative Methodik findet Anwendung in der Strukturbiologie, der Evolutionsbiologie und verwandten Bereichen.“
-
Eine Methode zur genetischen Charakterisierung von Krebszellclustern
Veröffentlicht in: Nature Genetics
Beteiligte SIB-Gruppe: Gruppe für Computational Biology unter der Leitung von Niko Beerenwinkel an der ETH Zürich
Beschreibung: Gruppen von Tumorzellen im Blutkreislauf können Metastasen bilden. Ein neuer Algorithmus ermöglicht die DNA-Sequenzanalyse einzelner Zellen innerhalb solcher Cluster – und liefert den ersten Beweis dafür, dass viele davon genetisch unterschiedliche Zellen enthalten. Die Methode ebnet den Weg für weniger invasive Diagnostik.
Das Komitee sagte: „Durch die Lösung eines anspruchsvollen Problems an der Schnittstelle von Phylogenetik und Einzelzellgenomik unterstreicht diese Arbeit die Leistungsfähigkeit der Bioinformatik als Motor für Entdeckungen in der biomedizinischen Forschung. Sie veranschaulicht zudem den Wert einer engen Zusammenarbeit zwischen experimentellen und computergestützten Wissenschaftlern.“
Entdecken Sie diese Veröffentlichung
-
Ein KI-Tool für eine schnellere und kostengünstigere Wirkstoffforschung
Veröffentlicht in: Nature
Beteiligte SIB-Gruppe: Labor für Proteindesign und Immunoengineering unter der Leitung von Bruno Correia an der EPFL
Beschreibung: BindCraft entwirft „Binder“-Proteine, die die Aktivität therapeutischer Zielmoleküle in einem einzigen Rechenschritt modifizieren – wodurch die Notwendigkeit groß angelegter experimenteller Screenings entfällt. Das Open-Source-KI-Tool ist bereits weit verbreitet und hat sich unter anderem bei der Blockierung von Allergenen und der präzisen Ausrichtung von Gentherapien bewährt.
Das Komitee sagte: „Diese innovative Methode stellt einen bedeutenden Fortschritt für das Proteindesign dar. Indem sie die Entdeckung von Bindeproteinen zu einem zuverlässigen rechnergestützten Prozess macht, eröffnet sie neue Möglichkeiten für das therapeutische Design und Innovationen in der Biotechnologie.“





![Peer Bork giving a talk at the [BC]2 Basel Computational Biology Conference](/sites/default/files/styles/card_image/public/2026-01/Peer-Bork_banner.jpg?h=602a36b5&itok=KM0WZZWK)