Eine internationale Forschergruppe fordert eine bessere Integration von Virusgenetik, Bioinformatik und öffentlicher Gesundheit, um Pandemien besser bekämpfen zu können und die Vorsorge für künftige Pandemien zu verbessern. In einem Kommentar in der Fachzeitschrift Nature zeigen eine internationale Gruppe von Spezialisten für Virus- und Genanalyse unter der Leitung der Schweizer Wissenschaftler Dr. Emma Hodcroft von der Universität Bern und Prof. Christophe Dessimoz von der Universität Lausanne, beide vom SIB Swiss Institute of Bioinformatics, sowie Dr. Nick Goldman vom EMBL-EBI im Vereinigten Königreich, die «bioinformatischen Engpässe» auf, die die Reaktion auf die SARS-CoV-2-Pandemie behindern, und schlagen Wege vor, um den Weg für bessere Instrumente und Ansätze zu ebnen. Hier sind die wichtigsten Erkenntnisse und Perspektiven aus Schweizer Sicht.

„Was Wissenschaftler in einem Jahr seit der Entdeckung eines völlig neuen Virus erreicht haben, ist wirklich bemerkenswert“, sagt Emma Hodcroft vom Institut für Sozial- und Präventivmedizin (ISPM) der Universität Bern, Erstautorin des Artikels, „aber die Instrumente, mit denen Wissenschaftler untersuchen, wie sich SARS-CoV-2 überträgt und verändert, wurden nie für die besonderen Belastungen – oder Datenmengen – dieser Pandemie.“
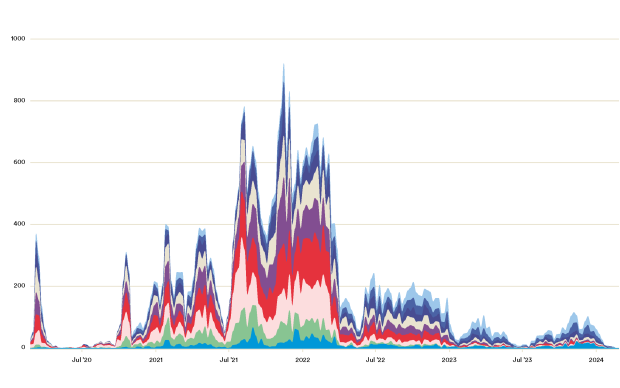
SARS-CoV-2 ist mittlerweile einer der am besten sequenzierten Krankheitserreger aller Zeiten: Seit Beginn der Pandemie wurden über 600.000 vollständige Genomsequenzen erstellt, und täglich kommen weltweit über 5.000 neue Sequenzen hinzu. Die heute verwendeten Analyse- und Visualisierungstools (darunter Nextstrain, das von der Gruppe um Prof. Richard Neher an der SIB und der Universität Basel mitentwickelt wurde) waren jedoch nie dafür ausgelegt, die Menge und Geschwindigkeit der heute generierten Sequenzen oder das Ausmaß der Beteiligung an Maßnahmen im Bereich der öffentlichen Gesundheit zu bewältigen. „Weltweit beruht die Überwachung des Virusgenoms auf der Initiative akademischer Forscher, die nach wichtigen Antworten suchen. Die Entscheidungsfindung im Bereich der öffentlichen Gesundheit würde von einem nachhaltigeren Rahmen für die Zusammenarbeit profitieren“, sagt Christophe Dessimoz von der SIB und der Universität Lausanne.
Was eine verbesserte Sequenzierung ermöglichen würde
Die genetischen Sequenzen von SARS-CoV-2 enthalten wertvolle Informationen für die Umsetzung wirksamer Pandemie-Maßnahmen und um dem Virus einen Schritt voraus zu sein. Durch den Vergleich der Anzahl der Mutationen, die verschiedene Proben gemeinsam aufweisen, können Wissenschaftler beispielsweise die Übertragung des Virus verfolgen und so Superspreading-Ereignisse und die internationale Ausbreitung identifizieren. Derzeit ist es jedoch schwierig, diese genetischen Informationen mit anderen wichtigen Variablen zu kombinieren – beispielsweise wer an einer Veranstaltung teilgenommen hat und wann Symptome aufgetreten sind –, die diese Methoden noch aussagekräftiger machen könnten.
Die „R-Zahl” hat sich im letzten Jahr von einem wissenschaftlichen Begriff zu einem Begriff entwickelt, der in aller Munde ist – sie gibt an, wie viele Menschen eine infizierte Person im Durchschnitt ansteckt. Auch hier können Sequenzen helfen, indem sie dabei helfen, importierte Fälle von lokalen Übertragungen zu unterscheiden. Dies ermöglicht eine genauere Schätzung von Re, erfordert jedoch ein hohes Maß an Sequenzierung und komplexe Analysen, die derzeit noch nicht flächendeckend durchgeführt werden.
Schließlich ist die Sequenzierung die einzige Möglichkeit, die vielen Mutationen zu identifizieren und zu verfolgen, die bei SARS-CoV-2 auftreten. Mutationen sind zwar ein normaler Teil des Viruslebens, aber Wissenschaftler müssen wissen, welche Varianten harmlos sind und welche die Übertragbarkeit oder den klinischen Verlauf des Virus verändern könnten. Die Kombination von Sequenzen, Laborarbeit und computergestützten Vorhersagen könnte zu einem besseren Verständnis der Auswirkungen von Mutationen führen, aber es gibt kaum Rahmenbedingungen, die die Zusammenarbeit dieser verschiedenen Fachgebiete erleichtern. „Die Virusdaten – Sequenzen und zugehörige Metadaten – müssen dank stabiler Infrastrukturen, die mit den Grundsätzen offener Daten kompatibel sind, ermittelt, gesammelt und harmonisiert werden, um die Begutachtung durch die Fachgemeinschaft und ihre Wiederverwendung zu erleichtern“, sagt Christophe Dessimoz von der SIB und der Universität Lausanne, Letzter Autor des Artikels.
Vorteile für die Schweiz
„In der Schweiz könnte die Bevölkerung von einer systematischeren und repräsentativeren Sequenzierung profitieren, beispielsweise durch eine bessere Kontaktverfolgung, gezielte Isolierung und Quarantäne kleinerer Regionen sowie die Schließung und Öffnung von Schulen auf der Grundlage des Auftretens bestimmter Varianten“, erklärt Emma Hodcroft.
Die Harmonisierung der Gesundheitsdaten ist ebenfalls ein wichtiges Thema. Die Schweiz unternimmt bereits auf nationaler Ebene grosse Anstrengungen durch das Swiss Personalized Health Network (SPHN). Die Forschenden sind überzeugt, dass das Potenzial der Schweiz in Bezug auf Fachwissen und Infrastruktur nur darauf wartet, zum Wohle der öffentlichen Gesundheit genutzt zu werden. «Die Instrumente für die Forschung sind vorhanden, und die Forschenden haben sich selbst organisiert und den ersten Schritt getan: Um diese Bemühungen auszuweiten und aufrechtzuerhalten und so Forschung und öffentliche Gesundheit näher zusammenzubringen, sind wir auf eine nachhaltige öffentliche Finanzierung angewiesen», sagt Christophe Dessimoz.
Reference(s)
Emma B. Hodcroft, Nicola De Maio, Rob Lanfear, Duncan R. MacCannell, Bui Quang Minh, Heiko A. Schmidt, Alexandros Stamatakis, Nick Goldman & Christophe Dessimoz : Pandemievarianten schneller verfolgen? Den Engpass in der Bioinformatik beseitigen. Nature Comment, 1. März 2021.