Une collaboration interdisciplinaire entre le groupe Christian von Mering du SIB et le groupe de recherche Sigel Lab de l'UZH a permis d'identifier le rôle d'une nouvelle molécule d'ARN présente dans les virus qui s'attaquent aux bactéries vivant dans notre intestin. À l'aide des données du projet Microbe Atlas, ils ont mis au jour un mécanisme utilisé par les bactériophages pour garantir le succès de leur infection dans la course à l'armement constante qui les oppose à leurs hôtes bactériens. Ces résultats offrent une nouvelle perspective sur la régulation de la flore intestinale et élargissent les connaissances générales sur la santé intestinale.
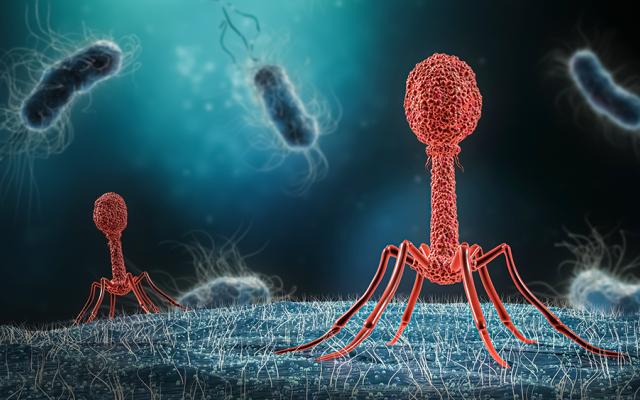
Dans le monde complexe de l'intestin humain, des milliards de micro-organismes jouent un rôle essentiel. Parmi eux, les bactériophages, des virus qui infectent les bactéries, suscitent un intérêt particulier chez les chercheurs. Comprendre comment les phages interagissent avec leur cible au niveau moléculaire ouvre de nouvelles perspectives pour la recherche biomédicale et permet de mieux comprendre comment l'équilibre du microbiome intestinal est maintenu ou perturbé en cas d'infection.
À propos du projet Microbe Atlas (MAP)
En regroupant et en analysant une vaste collection d'échantillons métagénomiques, MAP facilite l'identification et l'étude de populations microbiennes inconnues ou peu étudiées. Il fournit aux chercheurs des informations sur l'abondance typique et les environnements préférés (par exemple, volcan, océan, etc.) de ces microbes, sous forme de fiches techniques accessibles depuis l'interface web.
MAP est l'une des nombreuses ressources bioinformatiques développées par le groupe SIB de Christian von Mering. Parmi celles-ci, STRING, une base de données de pointe sur les interactions protéine-protéine, fait partie du portefeuille de ressources de données ouvertes du SIB.
Nouvelle perspective sur les interactions microbiennes
Les équipes ont identifié un sous-groupe de minuscules molécules d'ARN, appelées ribozymes thêta, au sein des bactériophages. Ces petites enzymes peuvent effectuer des coupures spécifiques pour libérer les ARN de transfert, qui permettent aux bactéries de comprendre et d'assimiler le code du virus. Le phage peut désormais adapter son propre matériel génétique et manipuler l'hôte sans qu'il s'en aperçoive, ce qui augmente ses chances d'infection.
À propos du projet Microbe Atlas (MAP)
En regroupant et en analysant une vaste collection d'échantillons métagénomiques, MAP facilite l'identification et l'étude de populations microbiennes inconnues ou peu étudiées. Il fournit aux chercheurs des informations sur l'abondance typique et les environnements préférés (par exemple, volcan, océan, etc.) de ces microbes, sous forme de fiches techniques accessibles depuis l'interface web.
MAP est l'une des nombreuses ressources bioinformatiques développées par le groupe SIB de Christian von Mering. Parmi celles-ci, STRING, une base de données de pointe sur les interactions protéine-protéine, fait partie du portefeuille de ressources de données ouvertes du SIB.
En suivant l'abondance des théta ribozymes dans des échantillons enregistrés dans le projet Microbe Atlas, les chercheurs ont pu confirmer la présence de ces enzymes ARN spécifiques dans les bactériophages présents dans l'intestin des humains et d'autres mammifères.
Apprivoiser les phages pour faire avancer la science
Comprendre comment les virus peuvent manipuler leur propre matériel génétique pour tromper leur hôte ouvre de nouvelles perspectives aux chercheurs dans le domaine biomédical. Développant leur méthode, Lukas Malfertheiner et Kasimir Kienbeck, doctorants dans les groupes de recherche respectifs et coauteurs principaux de l'étude, notent : « Nous avons été surpris de constater qu'il semble assez courant que les virus utilisent de petites ribozymes – certaines des molécules les plus anciennes connues – pour manipuler leurs hôtes bactériens. Cette découverte pourrait potentiellement être utilisée dans la phagothérapie, une alternative aux antibiotiques dans la lutte contre la menace croissante des pathogènes multirésistants. »
Reference(s)
Kienbeck, K., Malfertheiner, L., Zelger-Paulus, S. et al. Identification de ribozymes thêta de type HDV impliqués dans le recodage à base d'ARNt des bactériophages intestinaux. Nat Commun 15, 1559 (2024).